Ionización

La ionización es un proceso químico o físico que consiste en la producción de iones, las cuales poseen una carga eléctrica debido a la falta o exceso de electrones. De estos se produce el anión, que tiene una carga negativa, y el catión, que tiene una carga positiva.
Este proceso también está relacionado con la disociación electrolítica, un fenómeno donde una base, ácido o sal se disuelven en otro solvente generando iones. De la misma manera, estos pueden tener carga negativa o positiva.
El descubrimiento de este proceso se le atribuye al químico sueco Svante August Arrhenius, quien fue el primero en observar que ciertas sustancias en disolución se encuentran en forma de iones y no de moléculas. Su avance científico le valió la obtención del premio Nobel de Química.
Tabla de contenidos
En química

La ionización química es la que se emplea cuando otras técnicas de impacto electrónico no suministran información suficiente sobre un elemento o sustancia. Para ello, se utilizan diversos tipos de reacciones, de las cuales se pueden mencionar:
- Oxidación reducción: Se forma por medio de rompimiento de enlaces y donde dos sustancias ganan o pierden electrones. La parte que los pierde adquiere una carga positiva y la que la gana mantiene una carga negativa. Un ejemplo es la pila.
- Autoionización: Ocurre en moléculas de un mismo compuesto y aparece por el rompimiento o intercambio de átomos. Es la forma imperceptible de ionización, pues no tiene la habilidad de conducir electricidad.
- Ruptura heterolítica: Es cuando se rompe un enlace químico y los electrones se dirigen hacia el átomo con mayor afinidad. Esta es una de las reacciones que más se pueden observar a nivel orgánico.
En este tipo de ionización, los niveles de energía son más reducidos, aunque depende en gran manera del material reactivo utilizado. Además, en ocasiones no ocurre ninguna fragmentación, limitando la cantidad de información del elemento ionizado.
En física

La ionización también se encuentra en distintos procesos físicos y aparece cuando se le aplica energía. Consiste en aislar las moléculas a partir de irradiación, calentamiento o aplicación de un campo eléctrico. Algunos aspectos que caracterizan este proceso en física son:
- Los átomos de una materia se cargan eléctricamente sin perder la identidad original. Un ejemplo de ello es la electricidad estática, donde las superficies intercambian electrones cuando se frotan y una de ellas lo almacena.
- En los gases, si se les somete a un campo eléctrico, los átomos se mueven para liberar electrones. Luego, se enfrían, retornan a un estado menor de energía y despiden fotones. Así, se obtiene una fuente de iluminación a través de ionización gaseosa.
- Además, si se le aplica energía por distintos tipos de radiaciones a un elemento, gama o rayos ultravioleta, la energía desprende un electrón del átomo. Este tipo de ionización por radiación se observa en fenómenos cósmicos o radiactivos.
Una forma muy común de observar este tipo de ionización es en la desinfección o esterilización de las superficies. Gracias a su efectividad, reduce la carga microbiana en alimentos o insumos, evitando la proliferación de enfermedades.
Ionización del agua
La ionización del agua es un fenómeno que ocurre desde la antigüedad y se conoce como autoionización. Debe entenderse que el agua en su estado puro es un electrolito débil, por lo que su capacidad para conducir electricidad es muy baja, es decir, se ioniza muy poco.
Las bajas concentraciones de iones que posee son producto de la ionización que proviene de las moléculas de agua. Durante este proceso, algunas de estas moléculas actúan como ácidos y otras como bases, causando un intercambio de protones.
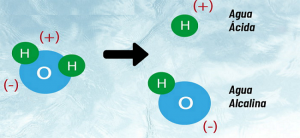
Entonces, cuando una molécula de agua (H₂O) es bombardeada por átomos cargados de iones o por fotones de suficiente energía, pierde uno de sus electrones. De esta manera, forma una especie con carga positiva, el ion H₂O+, el cual se considera constante.
Sin embargo, la constante del producto iónico del agua está directamente relacionada con los compuestos OH- como de H3O+ presentes en el líquido. La importancia de este nivel consiste en determinar si se puede convertir en una solución ácida, neutra o básica y con ello, el tipo de tratamiento que se le debe suministrar para lograr un objetivo.
Ionización del aire
El aire, por su parte, no posee autoionización como en el caso del agua. Las moléculas del nitrógeno, oxígeno, argón o los vapores de agua no intercambian átomos o electrones. Por tal razón, el aire no es un buen conductor de electricidad.

Sin embargo, se ha comprobado que cuando se somete a un campo eléctrico, temperaturas elevadas o radiaciones, puede ionizarse y ser un buen conductor de electricidad. Esto ocurre de forma natural en las nubes cuando los rayos eléctricos caen y de manera artificial con los equipos de purificación del aire.
Ejemplos
El fenómeno de ionización se encuentra en cada etapa de la vida diaria. Estos pueden ocurrir de forma natural o artificial, por lo que es un proceso que se puede observar en cualquier momento. Algunos de los ejemplos más comunes son:

- Esterilización por radiación: Muchos productos de consumo humano vienen en envases que han sido limpiados con rayos gamma, cuyas ondas causan la muerte de bacterias o microorganismos.
- Oxidación: Cuando los metales se oxidan por acción de una solución o del oxígeno ambiental, adquieren carga positiva para formar óxidos o sales. Por ejemplo, el hierro se convierte en óxido de hierro y el magnesio en sulfato de magnesio.
- Tubos de iluminación: En las lámparas de vapor o tubos de iluminación los átomos son estimulados con descargas eléctricas. Esto causa luz y colores, como es el caso de las luces de neón.
- Detección de explosivos y sustancias peligrosas.
En conclusión, la ionización es un proceso que se da en química y física, en las cuales hay un proceso de conversión que genera iones. Su efecto se puede ver en las actividades cotidianas y busca un equilibrio en el ambiente.
Referencias
1.quimica.es.-.Ionización, de Química.es. website:https://www.quimica.es/enciclopedia/Ionizaci%C3%B3n.html