Francio

El francio es un elemento químico radioactivo que pertenece a la serie de los metales alcalinos. En la tabla periódica se sitúa entre el radón y el radio. Posee una masa atómica de 223, es representado por el símbolo químico Fr y su número atómico es el 87.
El francio es un metal muy escaso en el planeta, solo se puede encontrar trazas de este elemento en minerales de uranio y de torio. En concreto, el radioisótopo francio-223 está continuamente creándose y desintegrándose en la naturaleza, produciendo astato, radio y radón.
Este metal alcalino radiactivo fue descubierto y aislado en 1939 por la física francesa Marguerite Perey, quien trabajó en el Instituto Curie. Perey logró purificar muestras de lantano que contenía actinio, el cual por decaimiento alfa (emisión de núcleos de helio) se transmuta en francio.
Tabla de contenidos
Características y propiedades

- El francio pertenece al grupo 1 de la tabla periódica.
- El francio es el elemento más inestable entre los 101 primeros elementos de la tabla periódica. Por ello, nunca se han producido una muestra lo suficiente abundante de francio para su estudio, por lo que ciertas propiedades son asumidas en función al patrón de la tabla periódica.
- El isótopo más estable del francio es el 223Fr, el cual tiene una vida media de 21,8 minutos, luego de los cuales se transmuta en astato-219 a través del decaimiento alfa, que es el único elemento radiactivo comparable a este en la naturaleza, con una vida media de apenas 56 segundos.
- Se conocen 34 isotopos del francio, de los cuales 32 son sintéticos, y todos ellos se desintegran en isótopos del astato, radio y radón. Los isótopos producidos en la naturaleza son el francio-223 y el francio-221, este último tiene una vida media de 4,8 minutos.
- Es un metal químicamente parecido al cesio.
- Por ser un metal alcalino se asume que tiene una alta reactividad.
- Por ser un metal muy pesado y porque su nivel de mayor energía solo puede ser ocupado por un electrón, posee el mayor peso equivalente de todos los elementos químicos.
- Es el segundo elemento más escaso en el planeta, siendo solamente superado por el astato.
Propiedades físicas
- Su punto de fusión es 27°C y su punto de ebullición es 677 °C.
- Su densidad es igual a 1870 kg/m3.
- A temperatura ambiente se encuentra en estado líquido.
- Es un metal paramagnético.
Propiedades químicas
- Su único estado de oxidación es +1, desempeñándose como una base fuerte.
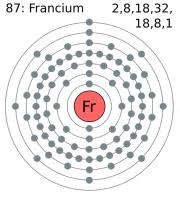
Configuración electrónica del Francio - Alta reactividad.
- El francio coprecipita al interactuar con el perclorato de cesio (también con el yodato, picrato, tartrato, cloroplatinato y silicowolframato de cesio y con el tartrato de rubidio), formando minúsculas cantidades de perclorato de francio.
- El francio también puede coprecipitar al interactuar con el ácido silicowolfrámico y con el ácido perclórico, sin que otro metal esté presente en la coprecipitación.
- La mayoría de las sales de francio son solubles en agua.
- Atómicamente, está compuesto por 87 electrones, 136 neutrones y 87 protones.
- Su nube de electrones oscila en 7 niveles energéticos.
Usos
El francio es un metal sin aplicaciones comerciales debido a su alta inestabilidad nuclear y a su escasez en el planeta.
No obstante, en el ámbito científico ha sido usado por propósitos investigativos en el campo de la química y en el estudio de la estructura atómica.
Los esfuerzos en el perfeccionamiento de la síntesis del francio han llevado a experimentos de espectroscopía especializada, que a su vez han conducido a la obtención de mayor conocimiento de los niveles de energía y las constantes de acoplamiento de partículas subatómicas.
Estudios acerca de la luz emitida por iones de francio-210 atrapados por láser han permitido obtener datos precisos de las transiciones entre niveles atómicos de energía, verificándose que estos coinciden con las predicciones de la teoría cuántica.
Dónde se encuentra
El isótopo más estable del francio, el francio-223, se produce en la naturaleza por medio del decaimiento alfa del isótopo actinio-227.
Además, pueden encontrarse trazas de francio-223 en los minerales de uranio y de torio. Se estima que en muestras de los minerales de uranio existe un átomo de francio-223 por cada 1x1018 átomos de uranio.
También se estima que en totalidad solamente existen 30g de francio en la corteza terrestre, en cualquier momento dado.
Obtención
El proceso más usado para sintetizar francio consiste en la inducción de una reacción de fusión al bombardear un objetivo de oro-197 con un haz de átomos de oxígeno-18, el cual es producido por un acelerador lineal. Este proceso fue desarrollado por la Universidad de Stony Brook en 1995.
Según sea la energía del haz de oxígeno, la reacción de fusión conduce a una cantidad dada de los isótopos 209Fr, 210Fr y 211Fr.
Entonces, los átomos de francio abandonan el objetivo de oro como iones, los cuales son neutralizados por colisión con átomos de itrio, para luego ser aislados en una trampa magneto-óptica (MOT), en un estado gaseoso no consolidado.
Pese a que los átomos de francio producidos solo se pueden almacenar por 30 segundos; tiempo después estos escapan o desarrollan decaimiento alfa, el proceso permite contar con un flujo continuo de nuevos átomos de francio.
El francio también puede ser producido bombardean radio con neutrones y bombardeando torio con protones, deuterones (núcleos de helio) o iones de helio. Incluso, el francio-223 puede ser aislado una vez se ha desintegrado una muestra de actinio-227.
Quién lo descubrió
Antes del descubrimiento del francio por Marguerite Perey en 1937, en el año 1870 los químicos sospechaban la existencia de un metal alcalino posterior al cesio, el cual debería tener el número atómico 87. A este, en aquel entonces, supuesto metal se le llamó eka-cesio.

Entre los años 1870 y 1937 ocurrieron varios intentos por concretar el descubrimiento y aislar al nuevo metal, pero la gran mayoría de estos fueron incompletos, y se ha confirmado que cuatro investigaciones llegaron a conclusiones erróneas.
Antes que el descubrimiento se le concediera a Perey, esta física tuvo una disputa con el químico rumano Horia Hulubei, que junto con su colega francesa Yvette Cauchois, afirmaba haber descubierto al eka-cesio al analizar espectroscópicamente una muestra de polucita con rayos X.
A pesar de que Hulubei tenía el apoyo de Jean Perrin, laureado Nobel y mentor del químico rumano, Perey atacó y dejó en evidencia los puntos débiles del trabajo de Hulubei, demostrando a la comunidad científica que el logro era suyo.
En el instituto Curie de París, Perey observó una discrepancia en la energía de desintegración de una muestra purificada de actinio-227. Después de descartar las posibles fuentes conocidas de alteración, llegó a la conclusión que se trataba de un nuevo metal alcalino, el eka-cesio.
Al isótopo que detectó en la muestra de actinio-227 lo llamó inicialmente actinio K, luego en 1946 propuso el nombre de catio, porque pensaba que era el catión más electropositivo de los todos elementos.
No obstante, el nombre catio no era del agrado de la física y química francesa Irène Joliot-Curie, supervisora de Perey, entonces le sugirió el nombre francium, en honor a su país natal.